北海道大学医学院 免疫科学講座 免疫生物学教室
教授清野 研一郎免疫科学講座
- 1991年、筑波大学医学専門学群卒業 外科コースに進む
- 1993~1997年、順天堂大学免疫学教室へ国内留学 日本学術振興会 特別研究員
- 1999年、筑波大学臨床医学系 講師(消化器外科)消化器癌及び臓器移植(腎臓、肝臓)の臨床と基礎研究に従事
- 2002年、理化学研究所免疫アレルギー科学総合研究センター 上級研究員
- 2006年、聖マリアンナ医科大学難病治療研究センター 准教授 部門長を経て
- 2010年、北海道大学遺伝子病制御研究所 教授
免疫チェックポイント阻害療法の効果を高める手法の発見
 免疫生物学教室では、移植とがんに関する免疫学的な研究に取り組んでいます。移植の分野ではiPS細胞からの免疫寛容源となるような細胞の誘導についての研究を進め、がんについてはがん微小環境における免疫抑制の仕組みや新しいがんワクチンについて研究を行っています。
免疫生物学教室では、移植とがんに関する免疫学的な研究に取り組んでいます。移植の分野ではiPS細胞からの免疫寛容源となるような細胞の誘導についての研究を進め、がんについてはがん微小環境における免疫抑制の仕組みや新しいがんワクチンについて研究を行っています。
「免疫は、感染症との関係性がよく知られていて、ワクチンを投与することによって感染症が排除できることがわかっています。がんに対しても同様に免疫が攻撃力を持つのではないかと考えられていますが、がんの仕組みについて解明されていないことも多く、がんと免疫の関係はそれほど単純ではないという考え方が主流でした」と清野研一郎教授。
がんに対する免疫療法の研究開発が本格的に進められるようになったのは2000年代以降のことで、2018年に京都大学特別教授の本庶佑氏がノーベル医学・生理学賞を受賞し、免疫チェックポイント阻害剤「ニボルマブ(商品名:オプジーボ)」が開発されたことにより、がん免疫療法が広く世に知られるようになりました。
「とはいえ、まだ解明しなければならないことが多く残されており、私たちはがんと免疫の関係性について、特に免疫チェックポイント阻害療法(Immune checkpoint blockade:ICB)[1]に着目し、ICBの治療効果を高めるための研究に取り組んでいます」。
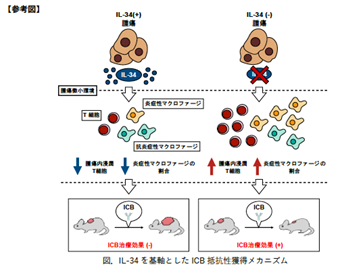
2020年、清野教授らの研究グループは、がん細胞が産生する液性生理活性因子インターロイキン-34(IL-34)が、ICBに対する抵抗性の獲得に寄与することを発見しました。IL-34は2008年に初めて同定された液性生理活性因子であり、正常なヒトにおけるその発現は、脳や皮膚に限定されることが知られています。また、清野教授らのグループは過去に、肺がん細胞由来のIL-34が、抗がん剤を用いた治療に対する治療抵抗性の獲得に寄与することを報告しました。しかし、多くのがん種が有するとされるICB治療抵抗性とIL-34の関係性は不明なままでした。
本研究では、マウス由来の3種のがん細胞を用い、IL-34の発現および作用を阻害することで、抗腫瘍効果を持つとされる炎症性マクロファージと、腫瘍細胞に対する攻撃の要であるT細胞の腫瘍内における割合が増加し、その結果、本来ICB治療に対し抵抗性を示していた腫瘍に対しても治療効果が得られるようになることを明らかにしました(図1)。IL-34を標的とした治療法は、他の治療法を組みあわせるとさらに治療効果が高まると考えられるので、これからのがん治療に大きく貢献できると期待されています。この研究結果は、IL-34とICB治療を紐づけた初めての報告であり、2020年9月19日公開のiScience誌にオンライン掲載されました。
再生医療における移植モデルを開発。細胞治療へのチャレンジもスタート
 iPS細胞を利用した移植医療の研究も、清野教授が長年取り組み続けているテーマです。iPS細胞は、色々な種類の細胞に性質を変えられるという特徴から、移植医療への応用が期待されています。しかし、他人由来 iPS細胞を移植に用いるときには、通常の移植医療と同様に移植を受けた患者さんの免疫細胞によって拒絶反応が引き起こされる恐れがあります。このリスクを低減するために、白血球の型を合わせた拒絶反応の起こりにくい組み合わせのiPS細胞を用いた移植が計画されていますが、どのような免疫応答がどの程度生じるかについてはこれまで検証されていませんでした。
iPS細胞を利用した移植医療の研究も、清野教授が長年取り組み続けているテーマです。iPS細胞は、色々な種類の細胞に性質を変えられるという特徴から、移植医療への応用が期待されています。しかし、他人由来 iPS細胞を移植に用いるときには、通常の移植医療と同様に移植を受けた患者さんの免疫細胞によって拒絶反応が引き起こされる恐れがあります。このリスクを低減するために、白血球の型を合わせた拒絶反応の起こりにくい組み合わせのiPS細胞を用いた移植が計画されていますが、どのような免疫応答がどの程度生じるかについてはこれまで検証されていませんでした。
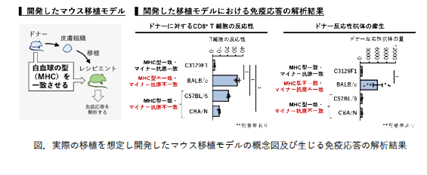
清野教授らの研究グループは、iPS細胞を利用したマウスの皮膚移植実験モデルを開発し、白血球型を一致させた移植であっても、T細胞が反応し拒絶反応が生じることを発見しました(図2)。さらに、このモデルを使って免疫抑制剤の有効性について検証し、長期間にわたって拒絶反応を抑制することができる移植の組み合わせがある一方、免疫抑制剤を使用しても移植片が拒絶されてしまう場合があることなどを示しました。この結果は、移植後に免疫反応の制御を行うことの重要性を改めて指摘するものとなっています。本研究成果は、2020年8月11日公開のScientific Reports誌に掲載されました。
また、最近は第3の研究テーマとして「細胞治療」の研究も開始しています。細胞治療とは、自分自身あるいは他人の「生きている細胞」を薬のように使って疾患の治療を行う手法です。清野教授は「近年は、アスピリンなどの低分子化合物だけでなく抗体やタンパク質などの高分子が薬として使われるようになってきています。その先にあるものとして、生きている細胞そのものを体内に注入するなどして治療を行う時代になってくるだろうと思います。生命科学の大きな流れとして細胞治療に可能性を感じ、本教室の重要な研究テーマのひとつとして本格的に取り組むことにしました。現在、免疫細胞を用いた細胞治療として肝線維症に対するマクロファージ療法を北大の消化器内科・消化器外科と共同研究を進めており、臨床試験の準備も始まっています」と語ります。
細胞治療は、がんや移植に限らずさまざまな疾患に対する新しい治療法として注目を集めている分野です。清野教授は、今後20〜30年のうちに、細胞治療が主流になってくると予想し、免疫生物学教室に所属する学生や若い研究者が細胞治療の研究に意欲的に取り組み、次世代の医療を牽引していくことを願っています。


[1] ^ がん細胞は、発がん過程において免疫チェックポイント分子を利用して免疫反応から逃避する働きを持つようになることから、その働きを阻害し、免疫反応を活性化させる治療法が免疫チェックポイント阻害療法(ICB)である。
(取材:2021年8月)
多彩な専門分野の学生・留学生・研究者が集まる場

免疫生物学教室に所属する学生は、北大内外、札幌内外、北海道内外、国内外からたくさんの学生が集まっています。出身学部も、医学部のみならず理学部や農学部、工学部などさまざまで、海外からの留学生も含めた多彩な人材がお互いに刺激しあっています。教授室にはギターやキーボード、アルトサックスなどの楽器が用意され、学生たちが演奏したり、教授を囲んで語り合ったりするなど、開放的な雰囲気があります。最近は、新型コロナウイルス感染症の影響で人が集まる機会が減ってしまいましたが、教員と学生、先輩・後輩が自由に交流する風通しの良さは現在も変わりません。